Embolización de aneurismas intracraneales mediante dispositivo diversor o disruptor de Flujo intrasacular “Woven EndoBridge” (WEB)
I. INTRODUCCION
Los aneurismas son evaginaciones focales, redondeadas o lobuladas, que normalmente se originan en las bifurcaciones arteriales. El saco aneurismático puede tener un orificio de entrada estrecho (cuello) o una base de implantación ancha que lo comunica con el vaso. Si excede los 2.5 cm de diámetro se denomina aneurisma gigante. Las causas de este padecimiento incluyen trastornos degenerativos o adquiridos, poliquistosis, colagenopatías, ateroesclerosis, traumatismo, infección (micosis), malformaciones arteriovenosas (MAV), vasculitis y fármacos. Son lesiones típicas de los adultos, con pico de presentación entre los 40 y los 60 años. El riesgo de ruptura es de 1-2% por año para aneurismas asintomáticos íntegros, existiendo una probabilidad mayor de ruptura en pacientes con aneurismas múltiples.
Los aneurismas intracraneales surgen normalmente en el polígono de Willis o en la bifurcación de la arteria cerebral media (ACM). Por necropsia, aproximadamente 90% tiene localización en circulación anterior y sólo 10% en el sistema vertebrobasilar. Un 33% de los aneurismas se localizan en la arteria comunicante anterior (ACoA), otro 33% en la unión de la arteria comunicante posterior (ACoP) con la arteria carótida interna (ACI) y 20% en la bifurcación o trifurcación de la arteria cerebral media (ACM).
Por angiografía, 38% se localizan en la ACoP, 36% en la ACoA, 21% en la bifurcación de la ACM, 2.2% en la bifurcación de la ACI y 2.8% en la arteria basilar. Siendo estas estadísticas norteamericanas, sin embargo, no existen estudios amplios o al menos publicados en la población mexicana sobre la localización y predominio de los aneurismas intracraneales en nuestro país.
Cognard refiere valores algo diferentes, menciona un predominio de los aneurismas en la ACI en 33%, seguido por la ACoA en 24%, la ACM en 21%, la vertebral en 17% y otras zonas en 6%.
Las complicaciones incluyen Vasoespasmo, provocado por la hemorragia subaracnoidea siendo la principal causa de muerte; Hematoma focal y efecto de volumen, pudiendo provocar neuropatías focales y herniación; Infarto, el vasoespasmo es la causa más común de infarto, sin embargo, la migración de material trombótico del aneurisma puede causar isquemia e infarto.
Resangrado, los aneurismas presentan un alto porcentaje de resangrado en las primeras 24 hrs después de la hemorragia inicial. De no tratarse, de 50 a 90% de los aneurismas resangran a los seis meses. El tamaño crítico para que un aneurisma sacular se rompa está entre los 4 y 7 mm, pero no existe un tamaño crítico por debajo del cual no se produzca una hemorragia subaracnoidea. El riesgo de sangrado es de 1-2% anual acumulativo; la ACoA es la que más riesgo tiene, siendo hasta de 70%, seguido por la ACoP. Los aneurismas localizados en los puntos de bifurcación son los que presentan mayor riesgo de sangrado.
II. MATERIAL Y MÉTODOS
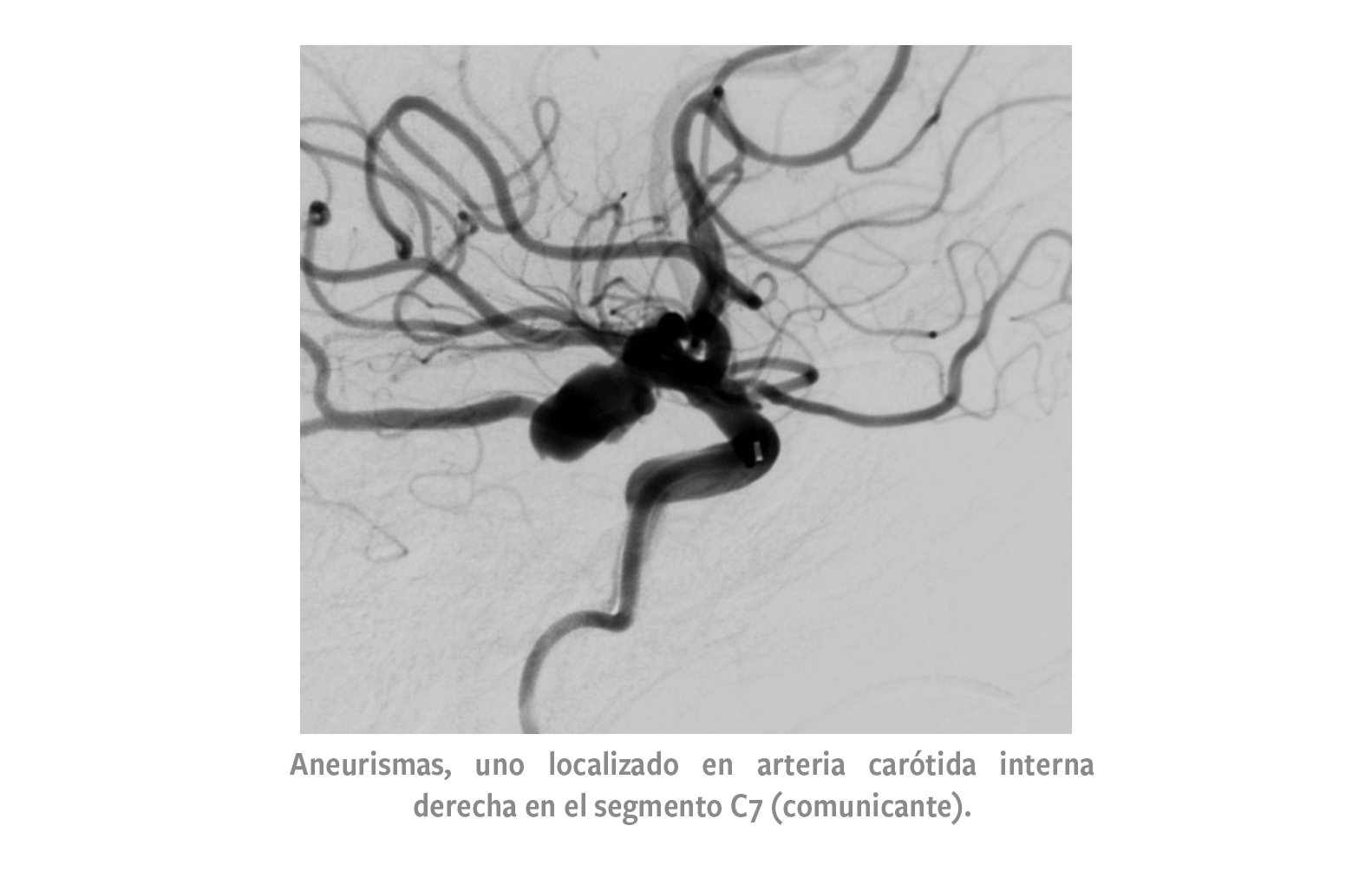
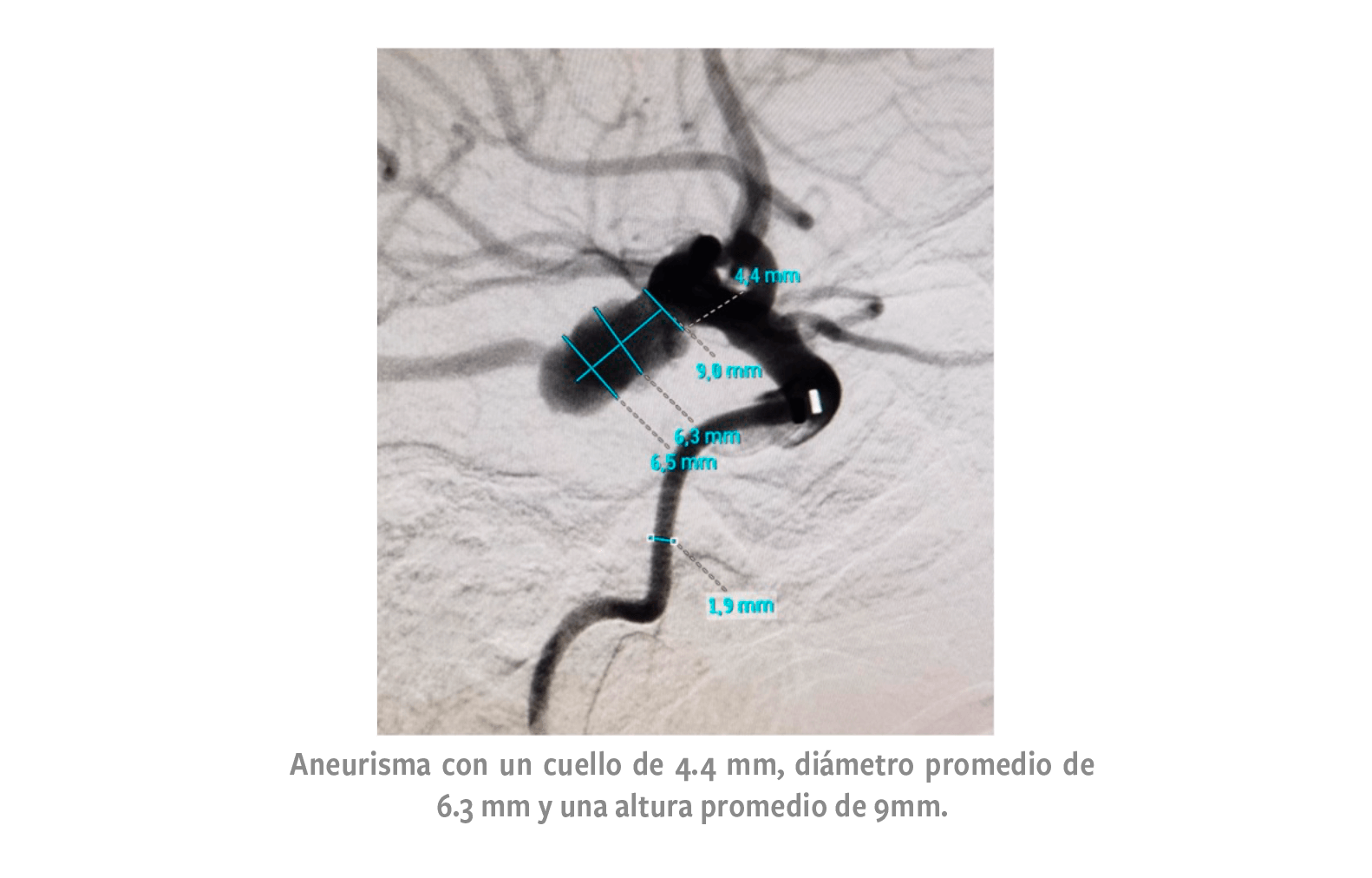
Paciente femenino, presenta 2 aneurismas intracraneales, el primero, localizado en arteria carótida interna derecha en el segmento C7 (comunicante) el cual poseía un cuello de 4.4 mm, diámetro promedio de 6.3 mm y una altura promedio de 9 mm.
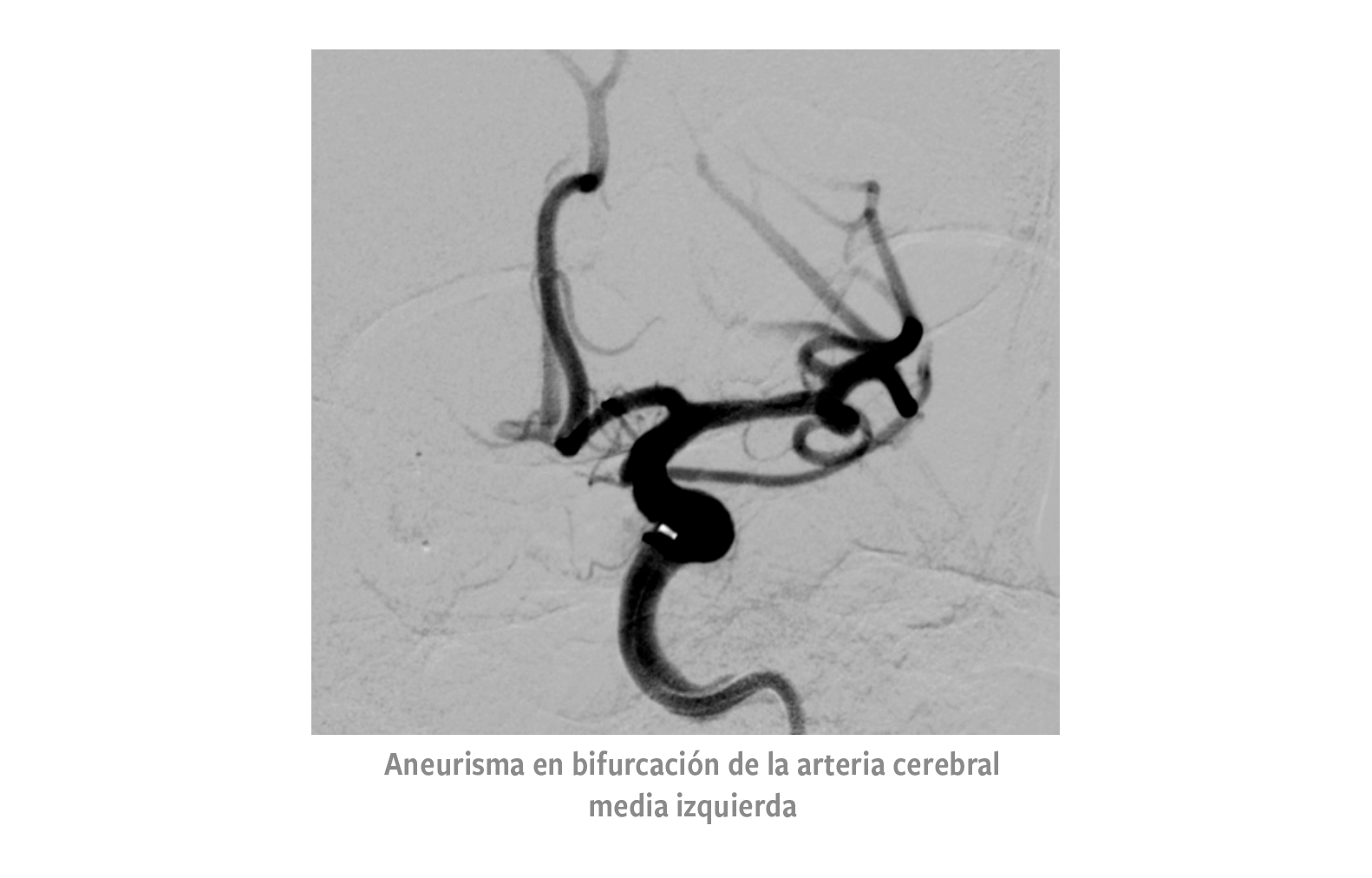
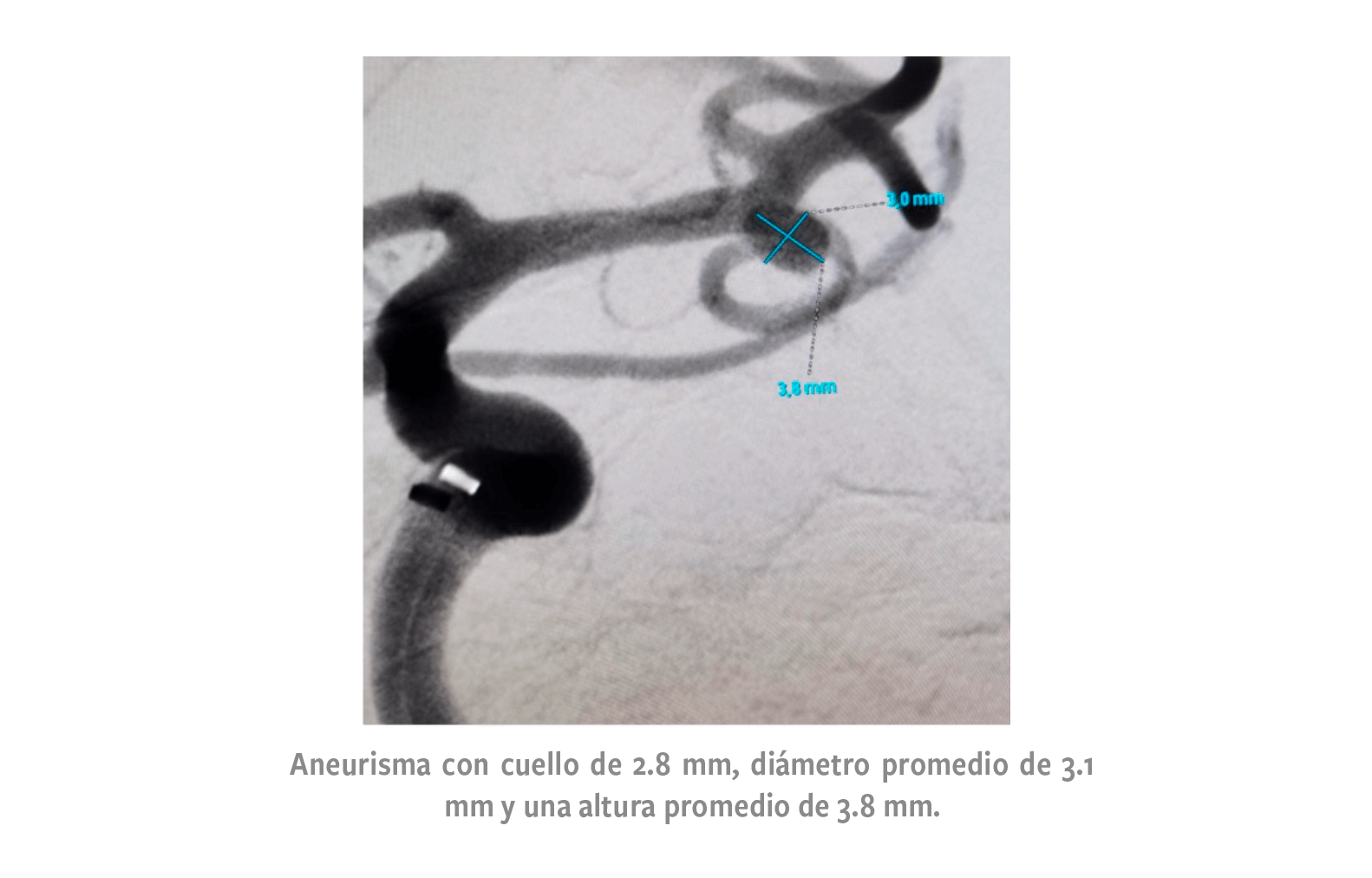
El segundo aneurisma se localizo en la bifurcación de la arteria cerebral media izquierda, el cual poseía un cuello de 2.8 mm, diámetro promedio de 3.1 mm y una altura promedio de 3.8 mm.
El tratamiento de ambos aneurismas se realizo mediante técnica endovascular mediante el dispositivo disrruptor de Flujo “Woven EndoBridge” (WEB), mediante sistema triaxial.
Para el calculo del dispositivo Woven EndoBridge” (WEB) que se requería en cada aneurisma utilizamos la técnica de estimación que detallaremos a continuación.
1. Medidas
Medir el aneurisma en al menos 2 proyecciones ortogonales (cuello, diámetro y altura).
2. Calculo de promedios.
A las medidas obtenidas respecto al diámetro, se calcula su promedio y se le adiciona un milímetro para la selección del dispositivo.
A las medidas obtenidas respecto a la altura, a la menor obtenida en proyecciones ortogonalesse le resta un milímetro para la selección del dispositivo.
3. Selección del dispositivo
Con las medidas obtenidas en los pasos anteriores, se selecciona el dispositivo apoyándonos con la tabla de selección.
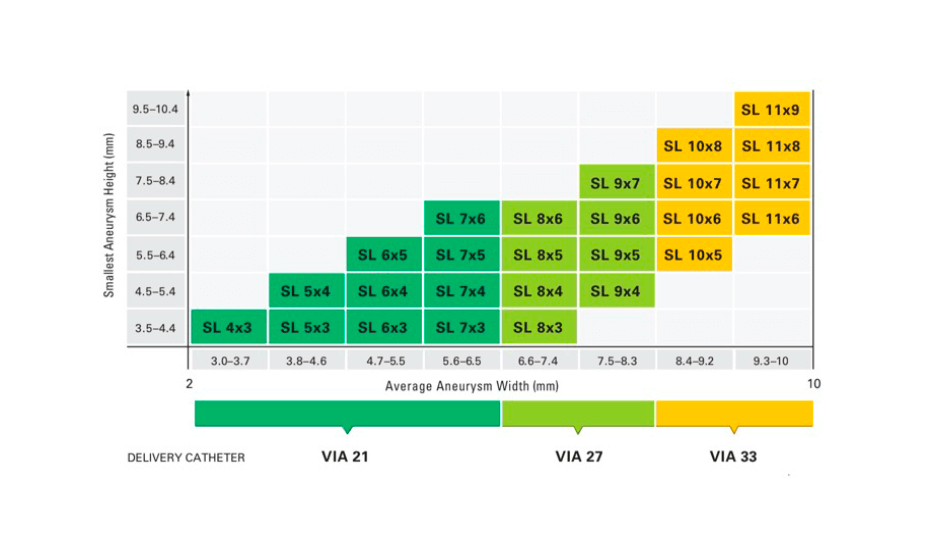
III. RESULTADOS
1. Selección de dispositivo “aneurisma de carótida interna derecha”
Para el aneurisma de arteria carótida interna derecha (imagen 3), se eligió el dispositivo WEB SL 10x6 (10 mm de diámetro y 6 mm de altura) respecto a las siguientes medidas.
• Diámetropromedio (Dp): 6.3 mm
• Alturaminima (Am): 9 mm
A) Selección del diámetro WEB (DW )
DW = Dp + 1 mm = 7.3 mm.
B) Selección de altura WEB (AW)
AW = Am – 1 mm = 8 mm
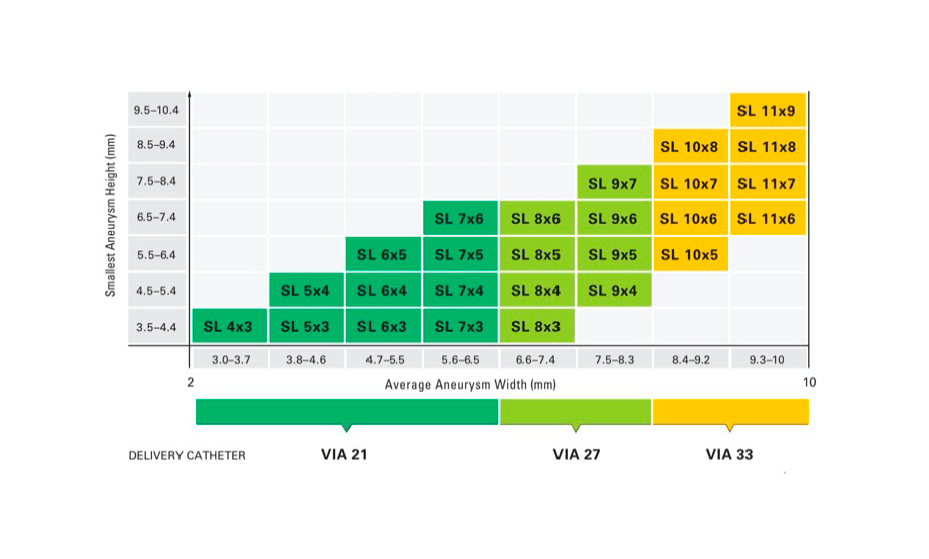
Como se puede observar en la tabla de selección, no existe dispositivo que cubra las necesidades del aneurisma respecto a las medidas obtenidas mediante sustracción angiografíca y a su morfología.
Teniendo en cuanta el nivel de adaptabilidad que posee el dispositivo y que cada milímetro de compresión lateral que sufre este, lo compensa, alongándose en altura, se selecciona el dispositivo WEB SL 10x6, el cual se adosara efectivamente a las paredes laterales del aneurisma teniendo una compresión de 4 mm, lo cual genera que el dispositivo crezca en altura hasta 10 mm de diámetro.
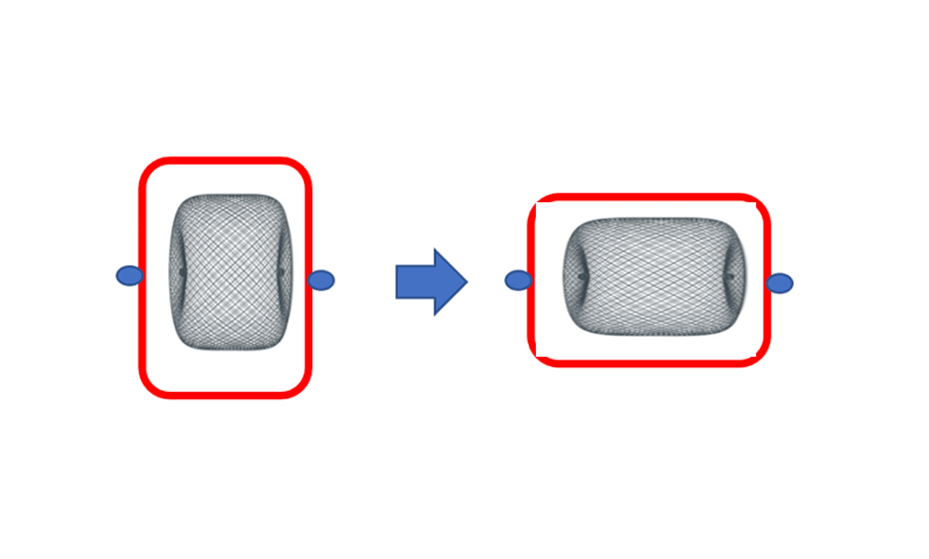
Como podemos observar en la imagen 6, poseemos un dispositivo con 10 mm de diámetro y 6 mm de altura, debido a la compresión lateral, que este sufre al encontrarse dentro del aneurisma, se convierte en un dispositivo WEB SL 6x10 (6 mm de diámetro y 10 mm de altura), esto se requirió así, ya que la mayor cobertura metálica se encuentra en los recesos del dispositivo generando así el efecto diversor o disruptor de flujo.
Ya con la selección de dispositivo obtuvimos el siguiente resultado.
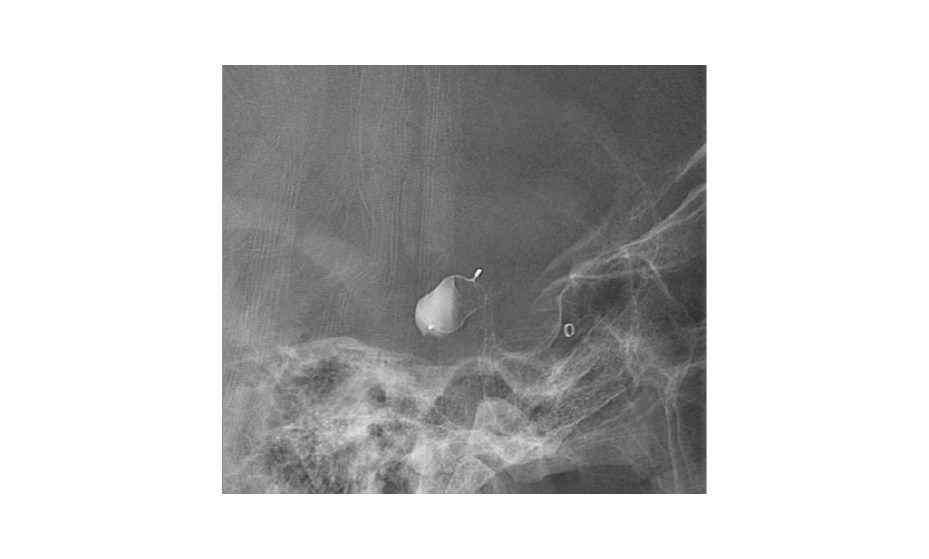
Como se puede observar, el dispositivo se adapto a la anatomia del aneurisma, con una correcta conpresion lateral y una cobertura del cuello con el dispositivo.
2. Selección de dispositivo “Aneurisma de bifurcacion de arteria cerebral media izquierda”
Para el Aneurisma de bifurcacion de arteria cerebral media izquierda (imagen 2), se eligió el dispositivo WEB SL 4x3 (4 mm de diámetro y 3 mm de altura) respecto a las siguientes medidas.
• Diámetropromedio (Dp): 3.1 mm
• Alturaminima (Am): 3.8 mm
C) Selección diámetro WEB (DW )
DW = Dp + 1 mm = 4.1 mm.
D) Selección de altura WEB (AW)
AW = Am – 1 mm = 2.8 mm
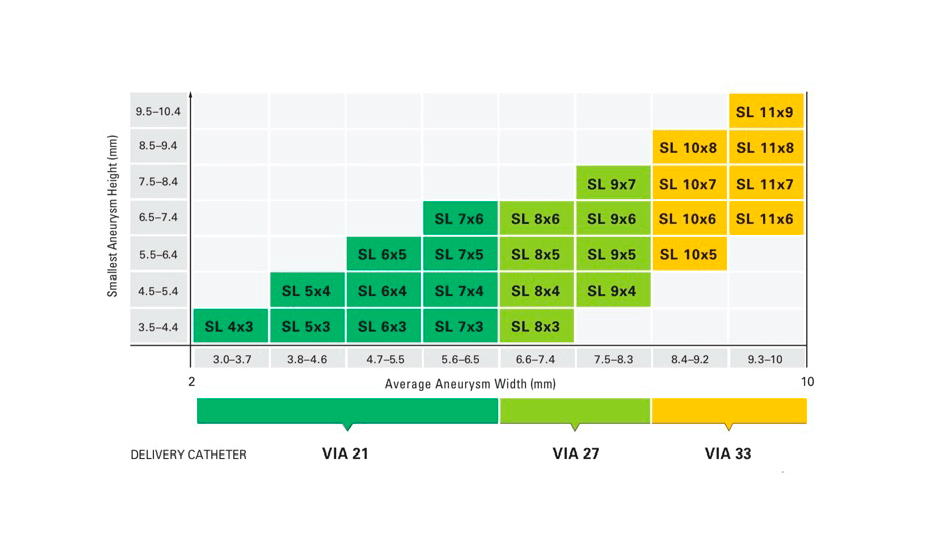
Como se puede observar en la tabla de selección, respecto a las medidas obtenidas mediante sustracción angiografíca y a la morfología del aneurisma se selecciona un dispositivo WEB SL 4x3.
Ya con la selección de dispositivo obtuvimos el siguiente resultado.
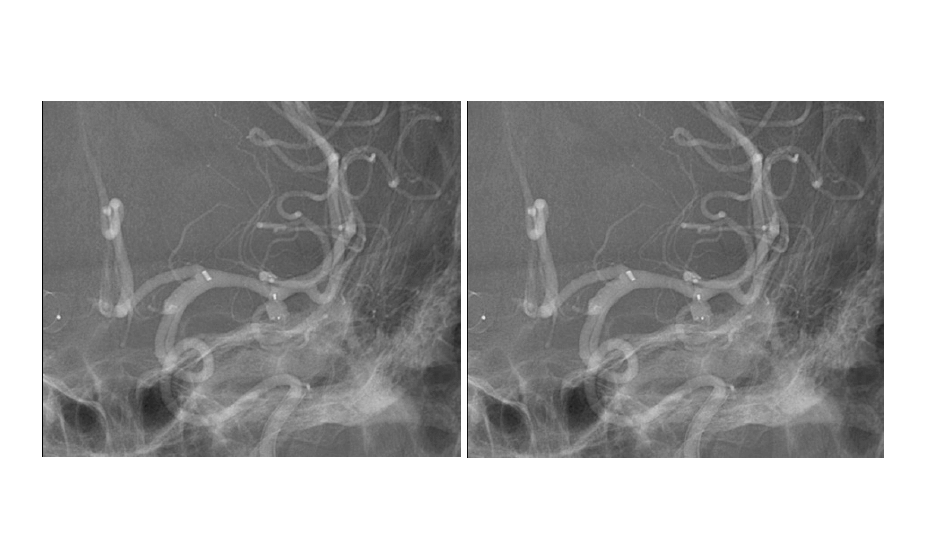
Como se puede observar, tenemos un correcto despliegue del dispositivo dentro del aneurisma, el cual presenta un correcto posicionamiento en las paredes y el cuello del aneurisma, de igual manera se observa que ambas ramas de la bifurcación de la arteria cerebral media izquierda se mantienen permeables y con flujo sanguíneo.
IV. CONCLUSIONES
El dispositivo “Woven EndoBridge” (WEB) representa una excelente alternativa en el tratamiento de aneurismas medianos de pared lateral y cuello ancho, rotos y no rotos, ya que evita el uso de doble terapia de antiagregación al tratarse de un dispositivo intrasacular y estar excluido del flujo sanguíneo.
En aneurismas de bifurcación, WEB, reduce la cantidad dispositivos auxiliares para su tratamiento, al solo requerir los diferentes catéteres de acceso y su microcatéter de liberación, minimizando los tiempos intraoperatorios y las dosis de radiación hacia el paciente, el personal de la sala de hemodinamia y al especialista en terapia endovascular neurológica.
De igual manera, la versatilidad y la capacidad del dispositivo de adaptarse internamente a diferentes morfologías, nos permite tratar una gran cantidad de aneurismas.
V. REFERENCIAS
1. Osborn A. Angiografía Cerebral. 2a Ed. Philadelphia, PA: Editorial Marban; 2000, p. 241-76.
2. Burgerner F, Meyers S, Tan R. Diagnóstico diferencial mediante resonancia magnética. 1a Ed. New York, NY: Ediciones Journal; 2005, p. 40, 53, 110, 124, 136, 174.
3. Cognard C, Weill A, Castaings L, et al. Intracranial Barry Aneurysms: Angiographic and Clinical Results after Endovascular Treatment. Radiology 1998; 206: 499-510.
4. Osborn A. Neuroradiología diagnóstica. Editorial Harcourt Brace; 1998, p. 248- 83.
5. Takao H, Nojo T. Treatment of Unruptured intracranial Aneurisms: Decision and Cost-effectiveness Analysis. Radiology 2007; 244: 755-66.
6. Dähnert W. Radiology Review Manual. 5a Ed. Editorial Lippincott Williams and Wilkins; 2003, p. 259-61.